郭旭峰医生的科普号
- 精选 食管癌多学科综合治疗:日本进展郭旭峰 副主任医师 上海市胸科医院 胸外科2170人已读
- 医学科普 肺部手术之后,身体会发生什么变化?(转自中山六院郑医生)
 郭旭峰 副主任医师 上海市胸科医院 胸外科340人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科340人已读 - 医学科普 促使磨玻璃结节长大、实变的幕后黑手到底是什么?(转自中山六院郑医生)
现在随着CT筛查的广泛开展,我们发现了各种各样的肺部结节,其中有一小部分会逐渐发展成肺癌。随着数据的积累,人们逐渐发现,尽管现有的循证医学证据都提示,早期肺腺癌的发展,可能是从非典型腺瘤样增生(AAH
 郭旭峰 副主任医师 上海市胸科医院 胸外科546人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科546人已读 - 医学科普 这种迂回曲折的治疗方案,可以大大提高肺癌患者的生存率(转自中山肿瘤郑大夫)
2022年1月26日,我临时起意写了个帖子,即《用4句话来总结肺癌外科治疗的20年发展》。原来开大刀,现在打小洞;原来治病重,现在治病初;原来只能手术,现在不用手术;原来不能手术,现在可以手术。从开大
 郭旭峰 副主任医师 上海市胸科医院 胸外科182人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科182人已读 - 医学科普 既然都要得新冠,为什么非要打疫苗?
2022.12.7,广州市召开最后一次疫情防控主题会,指出后续的新闻发布会将转向经济生活、常态化的发布会。2022.12.8,疫情防控新十条发布,指出应科学精准划分风险区域,不得采取任何形式的临时封控
 郭旭峰 副主任医师 上海市胸科医院 胸外科109人已读
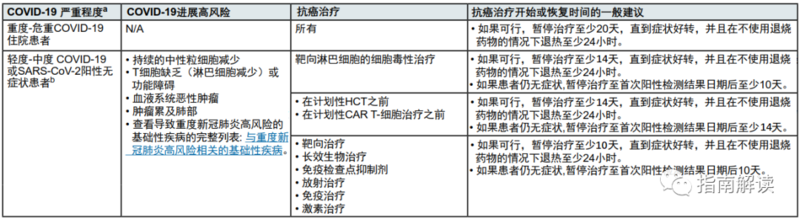
郭旭峰 副主任医师 上海市胸科医院 胸外科109人已读 - 医学科普 肿瘤患者“阳”了需要暂缓抗肿瘤治疗多久?有何应对策略?
近期,我国疫情防控政策陆续做了优化调整,许多地方已经取消常规核酸检测。据国家疾控中心和国内许多感染专家预测,放开后整体人群累计感染率将高达80%-90%;更长时间看,每个人可能至少都会经历一次感染。对
 郭旭峰 副主任医师 上海市胸科医院 胸外科855人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科855人已读 - 医学科普 磨玻璃结节选择消融前,你需要了解的事实(转自中山六院郑医生)
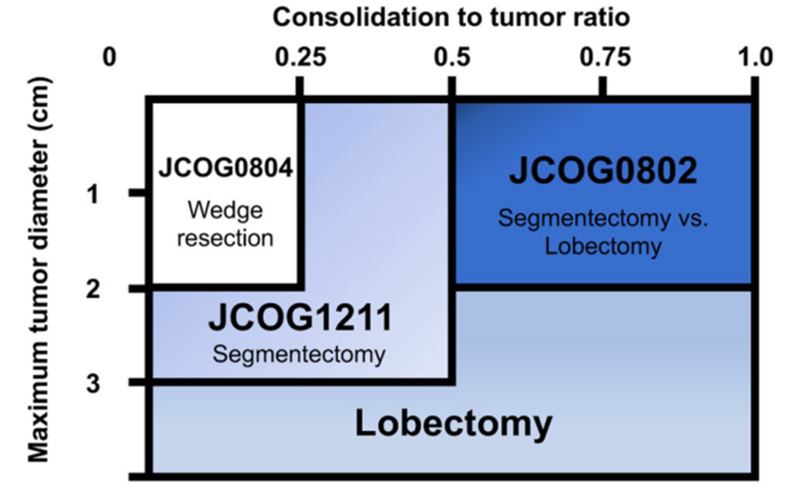
我依稀记得,当年我刚入门肺癌的时候,我的老师针对肺癌发病,给了我一个非常形象的比例,就是1比1比1。就是如果把全部初诊肺癌患者分为三份?那么有1份是早期肺癌,可以直接手术;有1份发生了局部进展,虽然做不了手术,但可以做放化疗;有1份发生了远处转移,连放化疗都做不了,只能做化疗。但是经过多年推广的肺癌筛查活动,现在早期肺癌的比例越来越多。2022年第十一届广州肺癌论坛上,天津市胸科医院胸外科主任张逊教授就分享了这么一组数据,即在可手术肺癌患者1958例中,病理一期占比59.1%。其中,IA期占比41.9%,IB期占比16.7%。不知不觉间,早期肺癌已经成为最大的那个群体。毫无疑问,肺癌发现越早,效果越好。在多年和早期肺癌相持的过程中,我们也逐渐反思,是否必须要采用最传统的肺叶切除进行治疗。毕竟因为一个一两厘米的癌结节就切掉整个肺叶,确实有点于心不忍。那到底能不能在确保疗效的情况下,实现最大程度的肺功能保留呢?于是我们有了JCOG系列研究,发现在基于肿瘤最大径与实性成分百分比筛选的合理人群,开展亚肺叶切除也是完全可以保证疗效的。这时,就有人会问这么个问题:面对早期肺癌,如果亚肺叶切除可以保证疗效,那热消融是不是也可以?于是我今天来尝试分析一下。研究分享#1 2020<IntJHyperthermia>第一个研究是2020年发表于国际热疗杂志的一项回顾性研究,探讨磨玻璃肺癌在微波消融治疗下的有效性。研究纳入103个磨玻璃结节,其中,纯磨玻璃84枚,混合磨玻璃结节19枚,全部采用微波消融进行治疗。最终,在平均18个月的随访期内,没有发生局部进展或复发。#2 2020 <JIntervMed>第二项研究是2020年发表于介入医学杂志上的一项回顾性研究。已经纳入20个磨玻璃肺癌,采用热消融治疗(包括微波和射频),最终,在平均16个月的随访期内,没有发生肿瘤的局部进展或复发。#32014 <JVasIntervRadiol>第三项研究是2014年发表于血管与介入放射学杂志的一项回顾性临床研究。研究纳入33名患者携带42枚磨玻璃为主型肺结节(14枚纯磨玻璃,19枚混杂磨玻璃),采用射频消融进行治疗。最终,在平均42个月的随访期内,有6个肿瘤出现了局部进展,其中四枚通过再次的消融治疗得到控制。直至随访结束,33名患者中,有31名没有肿瘤迹象。基于患者复发绘制的复发曲线显示,总体患者的1年复发率0%,3年复发率15.1%,5年复发率24.5%。#42020 <JVasIntervRadiol>第四项研究是2020年发表于,血管与介入影像学杂志的一项回顾性研究。研究纳入289名临床I期非小细胞肺癌患者,其中,193名给与亚肺叶切除,58名给予立体定向放疗技术(SBRT),38名给予射频消融。旨在是比较不同治疗手段的远期疗效。在随访时间方面,手术组平均分发时间53个月,立体定向放疗平均随访40个月,射频消融术平均随访时间53个月。生存分析显示,手术组的疗效普遍优于立体定向放疗和射频消融。5年生存率:手术vs立体定向放疗vs射频消融=85.5%vs42.0%vs58.9%;5年无进展生存率:手术vs 立体定向放疗 vs射频消融=75.9%vs34.9%vs39.9%但后续的比较发现,组间基线并不匹配。相比手术治疗组,接受立体定向放疗和射频消融的患者一般状况更差,而且肿瘤更大。于是,作者基于倾向性评分匹配,对三组患者的基线进行了校正。校正后发现,手术依然代表着最好的五年生存率和无进展生存率,但是组间的差异已经没有那么明显。5年生存率:手术vs 立体定向放疗 vs射频消融=71.0%vs63.7%vs59.7%;5年无进展生存率:手术vs 立体定向放疗 vs射频消融=61.9%vs55.7%vs35.9%热消融技术存在的问题热消融技术毫无疑问是一种非常有效的局部治疗手段,可以实现良好的肿瘤控制效果。但是跟手术相比,这个技术不论在临床开展还是数据研究,都比较局限。热消融技术,依然存在诸多问题亟待解决。这里面首当其冲的就是,到底是什么在影响着热消融技术的治疗效果。#5 2022 <JVasIntervRadiol>2022年10月发表于血管与介入放射学杂志上的一项研究,就指出太小的消融边界距离会干扰射频消融术的治疗效果。研究中,作者指出,针对射频消融患者,在消融后应该立即开展CT扫描以观察他们的消融有效范围。因为消融治疗后往往会导致肺组织充血而形成CT上的磨玻璃表现。此时,若磨玻璃范围完整的包绕肺结节,可以认定消融完全;而若磨玻璃范围不能完整包绕肺结节,则认定消融不完全。所谓消融边界距离,就是消融后的磨玻璃边界和肺结节边界之间的最小间距。基于此定义,作者纳入接受射频消融治疗的肠癌肺转移患者进行分析。发现在纳入的95名患者中,在消融后的6到19个月之间,有6例出现了局部复发。进一步的分析发现,较小的消融边界距离是导致他们复发的关键所在。在切缘距离不足2毫米的群体中,局部的复发率将明显增高,而多因素的分析也进一步证实了这个观点。#6 2018<IntJHyperthermia>另一项研究是2018年发表于国际热疗杂志上的一项真实世界研究。研究纳入68例已经提前知道病理类型的非小细胞肺癌患者,其中I-IIIA期35例,IIIB-IV期33例。在微波消融后立即开展粗针穿刺病理组织活检,并将穿刺病理与提前揭晓的组织病理进行匹配,基于匹配结果分为四个亚组。A组,穿刺取到相同的组织学类型(n=19)。B组,穿刺取到贴近的组织学类型,但伴有烧灼后的组织降解表现(n=28)。C组,穿刺组织无法确定具体病理类型(n=41)。D组,穿刺组织明确未见癌细胞(n=10)。最终分析发现,D组患者生存时间最长,中位无进展生存时间为26.6个月,中位总生存时间为29.8个月。而其他患者(A+B+C组)中位无进展生存时间只有11.7个月,中位总生存时间只有15.9个月。尽管受限于D组患者较小的样本量,最终的差异未达统计学意义(P=0.395),但这个研究无疑给我们一个很好的反思,即肿瘤消融治疗后的病理反应是否也会影响治疗效果。而如果这个假定是存在的,那我们又用什么手段去确保每次消融都能达到那种最佳的病理反应状态呢?毕竟,消融不同于手术,治疗以后的病灶依然长存于体内。第二个问题是,早期肺癌的热消融技术的效果是否足够可靠。针对这个问题,对应证据是前文提到的,编号为1、2、3的临床研究。尽管在前两篇2020年发表的研究中,都发现热消融可以在磨玻璃结节群体中取得非常满意的治疗效果,截至末次随访无一例复发,但这背后可能源自其较短的随访周期(平均随访时间,No.1-18个月,No.2-16个月)。而当随访时间延长以后,在第三篇2014年发表的那项研究中,42个磨玻璃肺癌采用热消融技术,有6枚肿瘤出现局部进展,3年复发率15.1%,五年复发率24.5%(平均随访时间,42个月)。从目前来看,要确定热消融技术在早期肺癌的具体疗效,我们还需要更多的临床数据,尤其是多中心、长随访的前瞻性临床研究。第三个问题,早期肺癌热消融技术能否实现跟手术相当的治疗效果。在这个问题目前没有头对头的临床对照研究,但从前面分享的编号为4的那项研究中,我们可以窥得一二。那项研究中,作者纳入289名临床I期非小细胞肺癌患者,分别给予亚肺叶切除术、立体定向放疗(SBRT)和射频消融治疗。在相对较长的随访间期后,比较了三种治疗手段的远期疗效。数据显示,在总体患者中,手术依然代表着最优的治疗效果5年生存率:手术vs立体定向放疗vs射频消融=85.5%vs42.0%vs58.9%;5年无进展生存率:手术vs 立体定向放疗 vs射频消融=75.9%vs34.9%vs39.9%即便在匹配后的患者中,手术的治愈率依然最高。5年生存率:手术vs 立体定向放疗 vs射频消融=71.0%vs63.7%vs59.7%;5年无进展生存率:手术vs 立体定向放疗 vs射频消融=61.9%vs55.7%vs35.9%。第四个问题,微波和射频应该如何选择。微波和射频,都是热消融的有效方式,都是通过诱导凝固性坏死的方式使细胞死亡。在技术层面,两者存在诸多区别:从研究数据来看,在编号#1研究中,总共有103个磨玻璃结节,采用微波消融,最后在18个月随访期内没有复发;而在编号#3和#4研究中,针对磨玻璃肺癌采用射频消融治疗后,在较长的随访周期内,都出现了复发事件。从技术层面看,微波消融可以在更段时间凝集更大的能量,也似乎更有助于杀灭核心区肿瘤细胞。但是,在2017年<肿瘤靶点(Oncotarget)>研究中,曾有研究者回顾分析了2007年接受热消融治疗的75名肺部肿瘤患者资料,包括射频消融术43例和微波消融32例。比较发现,两种治疗手段在肿瘤退缩率、总生存期和无进展生存期方面,并无明显差异。所以,尽管有一系列研究提示微波消融比射频消融更具优越性,但截至目前,尚无有效的临床数据可以证实该观点。热消融技术的专家共识2021年5月,《中国肺癌杂志》刊载了《热消融治疗肺部亚实性结节专家共识(2021版)》,描述了热消融治疗的适应人群和禁忌状况。共识指出,针对周围型磨玻璃结节患者,在出现以下情况后,可以考虑采用热消融技术:1.因心肺功能差或高龄无法耐受手术;2.本身拒绝手术治疗;3.手术切除以后又出现新的病灶或遗漏病灶,患者无法耐受再次手术或拒绝再次手术;4.多发磨玻璃结节;5.各种原因导致的重度胸膜粘连或胸膜腔闭锁;6.一侧肺缺如;7.重度焦虑经心理或药物治疗无法缓解。共识指出,在出现以下情况后,禁忌开展热消融技术:1.血小板<5010^9/L;2.有严重的出血倾向、短期内不能纠正的凝血功能障碍(凝血酶原时间大于18秒,凝血酶原活动度小于40%);3.严重的肺纤维化和肺动脉高压;4.抗凝治疗和或抗血小板药物在消融前停用未超过5~7天,贝伐珠单抗末次使用间隔未超过1个月。写在最后毫无疑问,热消融技术是一个充满光明发展前景的技术。其优异的肺功能保护和良好的局部控制效果,让他们可以成为,很多因各种原因而无法接受手术治疗的人群的,备选治疗选择。但我们也应该看到,热消融技术还需要进一步的成熟。在这个过程中,它还要堆砌更多的临床数据,积累更多的临床经验,摸索更加透明的可量化的评估标准。她是一颗坚硬的子弹,可以射穿任何铠甲。但要把她射准,我们需要更加娴熟的技能训练,更加稳定的枪身构造,以及更加可靠的瞄准准心。
 郭旭峰 副主任医师 上海市胸科医院 胸外科565人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科565人已读 - 医学科普 这样的实性肺癌,是很丑,可却很温柔(转自中山六院郑医生)
肺癌和肺癌是不一样的,从长相上,就很容易区分出来。比如,有的肺癌,长得像磨玻璃一样,这样的肺癌,病理成分中往往不含高侵袭成分,因此治疗效果很好。但有得肺癌,长得结结实实的,这样的肺癌,病理成分中的高侵
 郭旭峰 副主任医师 上海市胸科医院 胸外科436人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科436人已读 - 医学科普 继免疫之后的下一个风口:KRAS抑制剂?
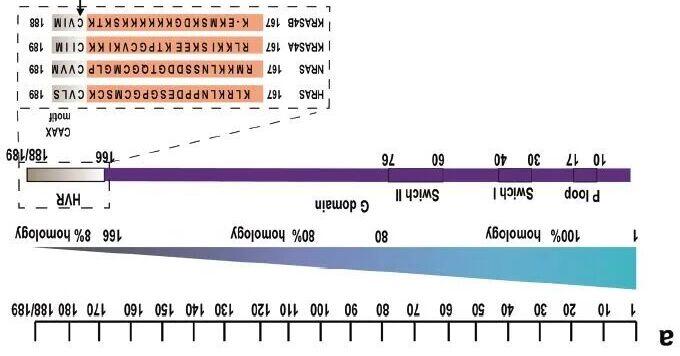
RAS家族包括KRAS,NRAS,HRAS,其中KARS最常见,占比85%左右;KRAS与很多恶性肿瘤相关,包括胰腺癌(突变率88%)、结肠癌(45-50%),非小细胞肺癌(35%)等,它是一种与鸟嘌呤核苷酸结合的膜结合调节蛋白,属于鸟嘌呤三磷酸酶(GTPases)家族,介导肿瘤细胞生长和增殖的细胞内信号通路。1.KRAS如何驱动肿瘤发生? 从结构上看,KRAS主要包括两部分:G结构域(Gdomain)和高变区(ahypervariableregion(HVR)),其中G结构域又由三段组成:switchI,switchII和Ploop。通常情况下,KRAS发挥分子开关的作用(图2),在不活跃的GDP结合状态(Inactive)和活跃的GTP结合状态(Active)间交替切换;而当细胞受到相关刺激时,KRAS与GDP的亲和力下降,然后GDP被具更高亲和力(大约10倍)的GTP取代,KRAS与GTP结合导致G结构域的switchI,switchII构象改变,然后KRAS被激活,以单体或二聚体的形式与下游分子结合,触发包括RAF-MEK-ERK(MAPK)通路在内的一系列信号级联反应。2.KRAS突变肺癌治疗现状KRAS突变更常见于肺腺癌(20-40%),较少发生于鳞癌(~5%)。以非小细胞肺癌为例,我们看到靶向EGFR的药物层出不穷时,过去四十年间事实上针对KRAS的研发却屡招滑铁卢,原因在于:(1)KRAS蛋白表面相对较浅和平滑,以传统的“锁钥模型”来看,由于缺乏凹槽,药物较难结合上去;(2)KRAS与GTP亲和力非常强,药物很难竞争性地结合上去和发挥抑制作用。 2013年,Ostrem,J.M.团队在Nature发文,KRASG12C亚型上存在一个变构调节位点(隐匿的凹槽)可被抑制(甘氨酸→半胱氨酸);于是针对该亚型的化合物设计和研发竞相开展,直到2021年AMG510率先上市,一举打破KRAS“不可成药靶点”的魔咒,取得里程碑式进展。 其作用机制为:Sotorasib(AMG510)通过与switchII下面的隐藏新口袋结合,将KRAS锁死在inactive或其与GDP结合的非活性状态,从而抑制KRAS蛋白活化和驱动肿瘤发生进展。CodeBreaK100II期研究于新英格兰杂志发文的数据显示:Sotorasib对于后线治疗的NSCLC患者客观缓解率(ORR)为37.1%,无疾病生存期(PFS)6.8个月,总生存期(OS)为12.5个月;20.6%的患者出现了≥3级的治疗相关不良事件(TRAEs)。另一KRASG12C抑制剂Adagrasib(MRTX849)近期在2022年ASCO报道了KRYSTAL-1研究数据,入组116例,意在评估Adagrasib(600mgBID,口服)用于既往接受过含铂化疗和抗PD-1/PD-L1治疗的KRASG12C突变NSCLC患者的疗效和安全性;主要研究终点是由盲法独立评审中心(BICR)评估(RECISTv1.1)的客观缓解率(ORR);截至2021年10月15日,中位随访时间为12.9个月,ORR为43.9%,PFS为6.5个月,OS为12.6个月;最常见的TRAEs为腹泻(63%)、恶心(62%)、呕吐(47%)、乏力(41%)、谷丙转氨酶(ALT)/谷草转氨酶(AST)升高(28%/25%)、血肌酐升高(26%),3-4级TRAEs发生率为43%,5级TRAEs2例(2%)。日前,Adagrasib的NDA已经在美国加速审批,MAA也已提交给欧洲药品管理局,有望成为全球第二个上市的KRASG12C抑制剂。3.未来展望对这些KRAS抑制剂的耐药机制分析和进一步提升药物疗效如协同放化疗、联合免疫治疗、靶向治疗、肿瘤代谢重塑等策略正处于临床研究中…2022WCLC报道了Sotorasib与SHP2抑制剂(RMC4630)的Ib期研究结果,总体人群ORR27%,初治患者ORR50%,安全性可耐受另一方面,KRASG12C抑制剂的成功案例初现曙光,但KRAS极度割裂,亚型众多,包括G12C、G12D、G12V突变等等。AnnalsofOncology和Naturemedicine先后发文报道G12D临床病理特征、基因特征分析和潜在KRASG12D抑制剂对药企来说,与其投资巨额成本逐一击破亚型、细分市场,不如选择直接进军主线,霸稳地位,研发泛KRAS抑制剂,Allin。Clinicaltrial公开数据显示,仅针对G12亚型,目前全球近70项临床研究正在进行中,且绝大部分处于recruiting状态,足以看出各大药企趋之若鹭此外,PROTEC技术的进步也为KRAS这一曾经不可成药靶点提供了更大的契机。总结 近年来,免疫治疗发展之迅猛的确不愧称作“一片蓝海”,今天也依然可见PD-1/PD-L1抑制剂还在不断扩大适应症,从进口药到国产药,从晚期肺癌到早期…不妨停下脚步思考,如何寻找有效的biomarker及提供耐药后治疗手段。 以2021年的KRASG12C抑制剂为例,靶向治疗稳扎稳打,从对基因特征分析、基础研究、到应用研究、到临床策略落地、最后到为增效和克服耐药而返回基因和肿瘤本质去发掘探索,这是一条完整的链条。靶向药物无疑比免疫治疗更贴近“精准治疗”的概念。KRAS突变在西方国家占比30%,亚洲地区约10%,市场潜力巨大,挑战与机遇并存。KRAS抑制剂是否会成为继免疫之后的下一个风口?拭目以待
 郭旭峰 副主任医师 上海市胸科医院 胸外科322人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科322人已读 - 医学科普 不用化疗的早期肺癌,手术以后要不要做基因检测?
现在早期肺癌的病人越来越多了,而且越来越趋向于年轻化。最近郑医生接诊的一个右下肺结节,手术做了。混合实性腺癌,22mm,无淋巴结转移,四十出头。从分期上来说,妥妥的早期,手术切了就可以,不用做术后辅助化疗。她很纠结,在做不做基因检测的问题上。做基因检测的目的是什么?肺癌一旦突破基底膜,就存在复发的风险。打个不恰当的比方,在面对存在复发风险的肺癌时,我们每个人的处境像极了狼牙山五壮士。面对一波波爬上来的鬼子(复发的肿瘤),我们只能一波波的打压下去,才能获得喘息的机会。这时候,武器就很重要了。在2009年之前,我们只能依靠放疗和化疗,因此大抵效果不好。但是,经过多年的发展,我们已经拥有了靶向治疗和免疫治疗两个重要手段,治疗效果也比原来不知道好了多少倍。只有当小米加步枪全部变成飞机加大跑,我们的狼牙山,那个最后的高地,才有被彻底守住的可能。但是,世界就是不公平的,虽然医疗水平进步了,但并不是每个人都可以平等享受。靶向治疗或免疫治疗都是有条件的。不加选择胡乱用药,很容易在没有获得疗效的情况下,却白白遭受副作用,即被药物反噬。而基因检测的目的,就是评估每个肺癌患者具不具备这种条件。提前做好基因检测,可以提前摸好条件,一旦考虑复发,就可以有效指导用药。所以,对这部分患者来说,基因检测的目的,是指导复发后用药。简单说来,因为可能复发,所以先做个检测备着。等复发以后再做行不行?基因检测一般都是很贵的,一次动则1w+,现在最先进的MRD检查甚至要2w+,而且没得报销。因此,有很多病友心里会犯嘀咕:“那既然我现在做了也指导不了这次用药,那就我以后等复发了,需要用药的时候再做不就完了,现在做有什么用?”这个观点,在逻辑上是没什么问题的。但是,真实情况往往不如人预想的那么理想。这里有两个最关键的干扰因素:一是时间、二是复发。在时间方面,早期肺癌目前手术完治疗效果是不错的,一般控制个几年是没问题的。目前的标本基本都是由石蜡封存的。经过长时间的保存,标本中的遗传信息并不会一直保持不变,简单说,就是会降解。最近,上海一位学者比较了2010、2015和2017年经由石蜡保存的子宫肌瘤标本,并提取其DNA进行分析。结果显示,保存时间更长的标本中的DNA降解更明显,提取出来的浓度更低。因为研究是2018年开展的,因此2017、2015、2010对应的保存时间分别是1年、3年和8年。如下图显示,保存时间更长的标本中的DNA降解更明显,提取出来的浓度更低。当以保存1年的DNA浓度为参照,保存3年和保存8年的标本其DNA浓度分别只有1年状态的80%和63%。而这些降解的DNA,势必会影响基因检测结果的准确性。简单说来,最有可能导致的一种误差,就是本来存在的一些突变,因为含量少被降解了,然后测不出来了。所以,基因检测报告上,都有这么一句话:“本次检测结果,仅对本次送检标本负责”。你送来的是啥样,我测出来的就是啥样,至于这个是不是你的真实情况,真的不是我能说了算的。但是,测得不准、漏测还不是最惨的,最惨的状况就是标本直接被打回来。因为标本放太久了,不合格,根本测不了(不敢测)。在郑医生认知范围内,国内绝大部分头部基因检测公司,不接受保存3年以上的石蜡标本。所以,这一下就尴尬了。因为早期肺癌手术效果基本都比较好,三五年不复发常有的事,结果等到将来要用的时候,你却告诉我,标本不能用了。第二个关键的因素,是复发。郑医生可以负责任的告诉你,在临床上,在没有取到病理标本获得绝对的病理诊断之前,任何的复发都是基于临床诊断。什么叫临床诊断?就是临床医生基于自身的临床经验以及患者的临床表现给出的诊断。这是有误差的。大专家可能大意失荆州,小医生也可能瞎猫碰上死耗子。因为,生活不是京剧,每个人都能带着脸谱上来,好人坏人可以一下子分清楚。肿瘤治疗也是一样。从理论上来说,一个复发型肺癌,在刚开始复发时就开始干预处理,那疗效应该就是最好的。但问题就是,这时候的复发病灶,它可以像炎症、像感染、像正常肺组织,但就是不像肺癌。甚至有一部分,影像学上没有明显的病灶,唯独肺癌标志物不明原因的异常升高。那怎么办?有人说,那就切下来看看。但是,一个人的肺组织都是有限、不可再生的,不可能因为一点点怀疑就去大动干戈切切切。也有人说,那就打化疗。但是,化疗药都是有反应的,有的反应还很大,盲目打化疗会严重影响个人的身体素质和免疫力。打对了,复发压下去,打错了,复发快起来。你敢赌吗?宁杀错不放过的治疗策略,在绝大多数临床医生看来,是一种很愚蠢的行为,跟自杀差不多。因此,临床上会采取一种更加稳妥的方法,就是密切随访观察。简单来说,就是复查的再频繁一些,等这些复发病灶长大了,看起来更像肺癌了,医生心里更有底了再处理。这时候,如果提前做了基因检测有靶向药吃,那就不一样了。因为绝大多数的肺癌靶向药副作用小,吃下去反应不大,但是却很有效果。因此,很多医生在面对这种模棱两可的状况,即虽然不能完全排除复发却又担心过分保守的随访导致病情进展,会推荐尝试吃一下靶向药再看,也就是诊断性治疗。这时候,那份当初看起来没什么用的基因检测报告,意义一下子就凸显起来。郑医生门诊就有一个早期肺癌术后患者,在术后3年左右出现了CT上的混合磨玻璃改变,合并有CEA不明原因升高,最高超过20,不能排除复发可能。但是,他术后做了基因检测,有EGFR突变,于是我就给他尝试吃了一段时间靶向药,结果病灶退缩,CEA回落。自此以后,这个病友就用CEA配合CT进行随访,迄今为止已经断断续续吃了快2年。所以,到底是做还是不做?可以说,早期肺癌做基因检测,为的就是给自己留一个后手。在抗击肺癌的过程中,如果每个人的手里都能多一把武器,那底气自然可以充足很多。所以,现在回到我们最初的那个问题:早期肺癌,到底要不要做基因检测?(这里的早期肺癌特指不用术后化疗的那种,即IA期及部分的IB期肺癌)郑医生有如下建议:如果本身病理类型是原位腺癌或微小浸润性腺癌,那么这类患者基本不会复发,因此基因检测是完全可以不用做的。如果本身病理类型是绝大多数的浸润性腺癌,那就要看个人的经济条件了。如果经济条件尚可,不至于做了以后影响日常生活,那就做吧,多抓一手牌,打起来更放心不是?但如果本身经济条件就不好,手术又掏掉家里的绝大部分积蓄,甚至贷款手术,再做基因检测会严重增加家庭经济负担,那就别做了吧。总结起来,基因检测做不做,看病情需要,也看经济条件。最后,那个纠结的病友结合自身拮据的经济条件,没有做基因检测。我觉得她做的对。眼前的状况都尚且自顾不暇,何必想那些几年以后才可能发生的问题呢?“白刃加胸,不计流矢”,你说对不?
 郭旭峰 副主任医师 上海市胸科医院 胸外科598人已读
郭旭峰 副主任医师 上海市胸科医院 胸外科598人已读





